- Вирусы, микробы, бактерии – что это такое?
- Вирусы
- Бактерии
- Микробы
- Что опаснее — вирусы или бактерии?
- Какие болезни вызываются вирусами?
- Чем отличается вирус от бактерии
- Какие болезни вызываются бактериями?
- Как уберечься от вирусов и бактерий?
- Врага нужно знать в лицо
- Гонка вооружений
- Наука и устойчивость
- Борьба с вирусами и бактериями
Вирусы, микробы, бактерии – что это такое?
Вирусы
Строго говоря, вирусы — это не совсем живые существа — ученые называют их неклеточными формами жизни или даже организмами, находящимися на грани живых. Это связано с тем, что вирусы1 не обладают важным свойством живых существ — клеточной структурой, присущей всем животным, растениям, грибам и бактериям. У них нет собственного метаболизма, поэтому они не могут жить одни. Для существования им всегда нужен другой организм, ведь вирусы — внутриклеточные паразиты.
Вирусы имеют размер от 20 до 350 нм (один нанометр составляет одну миллионную миллиметра). Самыми маленькими из них являются болезнетворные парвовирусы животных — всего 18 нм в диаметре. Вирусы гриппа крупнее: 80–120 нм. А возбудители оспы и трахомы вполне «гигантские»: достигают 300 нм и даже могут быть исследованы с помощью обычного светового микроскопа (а чтобы увидеть вирусы поменьше, нужен электрон).
Хотя вирусные заболевания всегда преследовали людей, сами вирусы по историческим меркам были открыты совсем недавно: их существование подтвердил в 1892 году российский микробиолог Дмитрий Ивановский. Будучи студентом, он изучал болезни растений и заинтересовался природой болезни табачной мозаики. После нескольких лет экспериментов Ивановский смог увидеть в оптический микроскоп группы возбудителя этого заболевания, после чего описал свои исследования в статье. А первый возбудитель вирусного заболевания человека — желтая лихорадка — был открыт только в 1901 году. И только в 1937 году было обнаружено, что против нее разработана вакцина, и эта болезнь уже несколько столетий убивает людей! С момента открытия вирусы активно изучаются, но большинство из них еще даже не систематизировано. Но новые вирусы появляются регулярно! При этом нет ни одной гипотезы происхождения вирусов, с которой согласились бы все вирусологи. Одни видят в них потомков доклеточных форм жизни, другие — «сбежавших» генетических структур, получивших некоторую независимость от клеток. Но количество всех вирусов на планете уже подсчитано: от 10 до 39 градусов больше, чем звезд во Вселенной. Прежде чем получить это число, ученые подсчитали 2, что более 800 миллионов вирусов накапливаются на одном квадратном метре нижней атмосферы Земли каждый день.
Вирусы очень лаконичны — по этой причине ученые когда-то считали их инертными кристаллами. Эти «кристаллы» имеют разный внешний вид: они могут быть сферическими, спиралевидными, продолговатыми. Но на самом деле любой вирус — это всего лишь оболочка, внутри которой находится генетический материал в виде молекул ДНК или РНК. Это «или» является важным различием между вирусом и нами, живыми существами: в наших клетках всегда есть и ДНК, и РНК. Но то, что нас объединяет с вирусом, — это желание приумножить наш генетический материал. Для этого вирусы должны проникнуть в живую клетку. Бывает, что вирусный геном просто вставляется в ДНК хозяина, и вирусу могут потребоваться годы, чтобы «проснуться». И если вирус проник в половые клетки и интегрировался в хромосомы, он будет передан потомкам хозяина. В геноме человека много таких включений (около 8%), полученных миллионы лет назад в ходе эволюции. Некоторые из них постепенно разрушаются, а другие оказались полезными для нас и участвуют в физиологических процессах. Например, в 2018 году ученые обнаружили 3, что вирусный ген играет жизненно важную роль в формировании нашей долговременной памяти.
Но что, если вирус не хочет прятаться, но стремится к активности? Таким образом, его генетический материал фактически перехватывает команду в живой клетке: он заставляет свои копии размножаться, которые все больше и больше проникают в ткани и органы. И во время этого «штамповки» происходит процесс, в результате которого вирусы приобретают репутацию коварных убийц. Новые вирусы не выходят со 100% копиями — некоторые из них выходят с «ошибкой», то есть с немного измененным геномом. Это вирусные мутации, которые помогают микроорганизму выжить, несмотря на усилия организма, который активно борется с инфекцией. Из-за мутаций вирусы могут выглядеть иначе и вводить в заблуждение иммунную систему: она должна заново ознакомиться с ней и разработать стратегию борьбы. Эту уловку активно используют вирусы гриппа, которые постоянно мутируют и приходят к нам каждый год в виде новых штаммов. Но наиболее удачная ситуация для вируса — это находиться в одной клетке со своими «коллегами» другого вида: например, когда встречаются вирусы от людей, птиц и обезьян. Затем они могут поменять местами целые части генома, и в результате получится принципиально новый штамм, мощный и опасный мутант, которого не остановят даже межвидовые барьеры: он может сначала заразить животное, а затем человека. Подобные вирусные эксперименты, как правило, проводятся в жарких, перенаселенных странах, где не очень хорошо с санитарией и люди чаще контактируют с дикими и сельскохозяйственными животными. Вот почему мы так часто слышим, что в Юго-Восточной Азии разразилась новая инфекция.
Бактерии
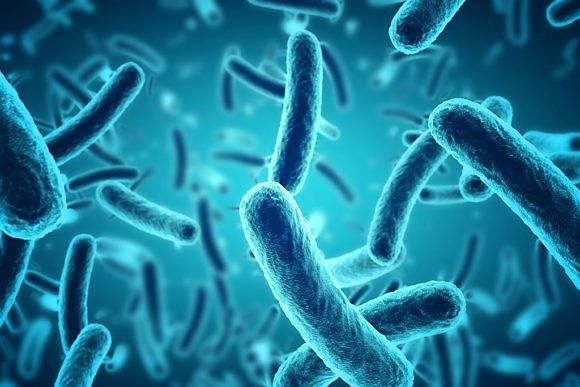
В отличие от вирусов, бактерии — самые живые организмы, хотя и очень маленькие (до 10 микрон, то есть одна сотая метра). Они одноклеточные, но эта клетка может иметь разную форму: бактерии круглой формы, в виде палочек, звездочек или кубиков, есть еще волнистые и С-образные. Структурно бактерии сложнее вирусов — у них есть клеточная стенка, структуры внутриклеточных, органелл и жгутиков для движения. Они живут и размножаются поодиночке (простым делением).
Бактерии — одни из первых обитателей Земли и самые распространенные: они также встречаются там, где никто не может выжить. Бактерии не боятся ни холода, ни кислотных источников, где температура воды почти 100 ° C.Они обитают в Мертвом море, в нижних слоях стратосферы, в Марианской впадине и даже в радиоактивных отходах. Ученые описали около 10 000 видов бактерий, но на самом деле их гораздо больше. Первые бактерии были обнаружены голландским ученым Энтони ван Левенгук в 1676 году. Он хотел выяснить, почему перец чили раздражает язык, и решил изучить настойку перца чили под микроскопом. Каково же было удивление натуралиста, увидевшего в крошечной капле движущихся существ! Левенгук назвал их «анимакули» и стал искать повсюду: в дождевой воде, на своей одежде, в царапинах собственных зубов. Он рассказал о своих наблюдениях в письме в Королевское общество развития знаний о природе. Но настоящий интерес к открытию Левенгука возник гораздо позже, в середине XIX века, когда начала развиваться клеточная теория.
Микробы
Когда вы говорите своему ребенку, что вокруг много микробов, вы не ошибаетесь. Микробы или микроорганизмы — это собирательное название всех живых существ размером менее 0,1 мм, которые нельзя увидеть невооруженным глазом. К ним относятся простейшие (микроскопические одноклеточные животные), бактерии и крошечные грибы, а также вирусы (не все ученые согласны с этим, поскольку вирусы еще не являются живыми организмами). Термин «микроб» объединяет греческое μικρό (маленький) и βίος — жизнь. Большинство микробов состоят из клетки, но некоторые из них являются многоклеточными.
Что опаснее — вирусы или бактерии?
Но на этот вопрос нельзя ответить: вирусы и бактерии могут быть как опасными, так и безвредными, в зависимости от ситуации. Большинство людей легко переносят сезонный грипп — ежегодное вирусное заболевание, но в начале двадцатого века испанский грипп унес, по разным оценкам, 3-5% населения планеты. Ужасные эпидемии прошлого — чума, холера, оспа — были вызваны бактериями, но каждый день мы спокойно контактируем с миллионами других бактерий. К началу июля 2021 года новая коронавирусная инфекция уже охватила более 182 миллионов человек во всем мире, при этом практика показывает, что, будучи изначально высокопатогенными, новые вирусы со временем становятся менее опасными. Как видите, опасность, которую представляют вирусы или бактерии, зависит от их «видовых» характеристик. Что касается устойчивости к вирусам и бактериям, в обоих случаях возникают трудности.
Если вирус уже проник в клетку, его нельзя убить — можно только ожидать, что организм с ним справится. Поэтому лучший способ борьбы с инфекцией — предотвратить заражение. Для этого есть вакцинация: во время вакцинации иммунитет знает вирус и заранее разрабатывает стратегию борьбы. Именно с помощью вакцин люди победили вирусные болезни, от которых когда-то не было спасения. Если сегодня мы вдруг начнем массово отказываться от прививок, то рискуем вернуться в прошлое — нас снова начнут поражать почти забытые болезни: оспа, корь, столбняк и так далее. Однако в случае вирусов, которые часто мутируют, вакцинация не всегда помогает. Вакцина может быть эффективной против одного штамма, но бесполезна против другого, более нового штамма. Вот почему ученые обратили внимание на возможности иммунитета. Его главное оружие в борьбе с вирусами — это белки интерферона, которые организм вырабатывает в ответ на вторжение. Они обладают неспецифическим действием, то есть действуют на широкий спектр вирусов. Интерфероны возникли в процессе эволюции и в настоящее время являются неотъемлемой частью противовирусного иммунитета. Однако интерферона может не хватить, это бывает по разным причинам: детский и пожилой возраст, наличие сопутствующих заболеваний, беременность и другие. Именно в этих случаях специалисты могут порекомендовать препараты на основе интерферона, такие как Виферон.
Люди тоже давно научились бороться с опасными бактериями с помощью антибиотиков (обратите внимание: они не действуют на вирусы, так как были разработаны для совершенно другой формы жизни!). Но есть еще одна проблема: со временем у бактерий вырабатывается устойчивость к ним. И чем чаще мы их используем, тем больше бактерий становятся к ним нечувствительны. Например, бактерии уже безразличны к пенициллину, с которого когда-то началась история антибиотиков. И все 80 лет прошло с момента его первого применения. Также разрабатываются новые антибиотики, но это очень трудоемкий и дорогостоящий процесс, поэтому существующие лекарства часто модифицируются.
Какие болезни вызываются вирусами?

Среди всех изученных вирусов (а их около 6000) очень небольшая часть является патогенной. Вирусные заболевания человека — грипп, корь, оспа, полиомиелит, эпидемический паротит, краснуха, герпес, инфекционный мононуклеоз, гепатит, энцефалит, СПИД и др. у животных — ящур, чума, бешенство. У растений есть различные мозаичные болезни и желтуха. Вообще говоря, вирусы не вредны и не полезны. Среди них наиболее важными для нас являются вирусы, поражающие только бактерии: их называют бактериофагами, то есть «пожирателями бактерий». Они используются в сельском хозяйстве для защиты животных и растений от бактериальных заболеваний. Также предполагается, что вирусы помогают жвачным животным превращать целлюлозу в сахара, которые затем превращаются в молоко или участвуют в увеличении веса. Еще одно достоинство фагов — регулирование количества бактерий в океане. Живущие там микроорганизмы производят почти половину кислорода Земли. Если один вид бактерий внезапно начнет бесконтрольно размножаться, вся пищевая цепочка будет нарушена, и многие виды просто не выживут. Некоторые вирусы стали важным компонентом симбиотических систем: естественных «партнерств», в которых организмы разных видов помогают друг другу. Например, трава растет на теплой почве возле гейзеров в Йеллоустонском национальном парке (США) 4, который выживает в экстремальных условиях только благодаря грибку, инфицированному определенным вирусом. А есть вирусы, которые замедляют развитие опасных заболеваний у людей: например, у людей, инфицированных гепатитом G, протекает легче, чем у другой инфекции — лихорадки Эбола, тоже вирусного заболевания. И вирусы от бактериальных инфекций тоже можно использовать: в СССР это практиковалось еще в 20-е годы прошлого века. Сегодня бактериофаги также «обучены» уничтожать рак — это называется вирусной онколитической терапией. Как видите, удаление вирусов — плохая идея, учитывая те преимущества, которые они предоставляют. Тем более, что это тоже невозможно теоретически: чтобы разработать универсальный вирусный яд, нужно сначала изучить абсолютно все вирусы. В краткосрочной перспективе это невозможно.
Чем отличается вирус от бактерии
Таким образом, и вирусы, и бактерии способны инфицировать организм, вызывая инфекционную инфекцию. Ключевое различие между ними заключается в механизме воспроизводства. Вирусы не могут воспроизводиться во внешней среде, поэтому они должны проникнуть в клетку. Бактерии размножаются путем деления и могут долгое время жить во внешней среде, ожидая попадания в организм человека. Следовательно, механизмы антибактериальной и противовирусной защиты также должны быть разными4.
- Размер и форма существования. Вирус — простейшая форма жизни, бактерия — одноклеточное живое существо.
- Жизнедеятельность. Вирус существует только внутри клетки и заражает ее, после чего размножается (клонирование). Бактерия живет полноценной жизнью, размножаясь делением, и организм для нее — лишь благоприятное место существования.
- Форма мероприятия. Вирусы, как правило, проявляются повышением температуры тела, общей слабостью, болями в мышцах и суставах. Бактерии проявляются в виде нездоровых выделений (гнойных или в виде специфического налета).
Типичные вирусные заболевания: ОРВИ, грипп, герпес, корь и краснуха. К ним также относятся энцефалит, гепатит, оспа, ВИЧ и др.
Типичные бактериальные заболевания: сифилис, коклюш, холера, туберкулез, дифтерия, тиф и кишечные инфекции, заболевания, передающиеся половым путем.
Бывает, что они оба вместе вызывают одно и то же заболевание. Этот симбиоз требует особого отношения. Примеры включают: синусит, тонзиллит, менингит, пневмонию и другие заболевания5.
Какие болезни вызываются бактериями?
Как и вирусы, бактерии5 могут быть безвредными для живых организмов или вызывать болезни. Такие паразитические бактерии попадают в организм и начинают им питаться, активно размножаются, повреждая клетки и отравляя их продуктами жизнедеятельности. Так начинается болезнь. У человека бактерии вызывают туберкулез, коклюш, менингит, чуму, сыпной тиф, столбняк, холеру, дифтерию, фурункулез, ангины. У животных — бруцеллез, сибирская язва. У растений подобная инфекция вызывает гниение, ожоги, пятна, увядание. Но есть еще много других полезных бактерий. Например, миллионы бактерий населяют наш кишечник, кожу и даже дыхательные пути. Их называют микробиотой, и ее баланс очень важен для поддержания здоровья: он создает условия, в которых вредные микроорганизмы не могут жить. Вы точно знаете две группы таких бактерий: это бифидобактерии и лактобактерии, обитающие в кишечнике.
Как уберечься от вирусов и бактерий?
В мире обитает огромное количество бактерий и вирусов, и избавиться от них совершенно невозможно, да и неразумно — ведь без них мы сами существовать не можем. Но предотвратить вирусное или бактериальное заболевание в повседневной жизни можно. Просто нужно соблюдать правила:
- соблюдайте гигиену, чаще мойте руки с мылом и реже прикасайтесь к лицу руками;
- сделать прививку;
- в разгар эпидемического сезона заболеваемости ОРВИ и гриппом используйте противовирусные препараты, например, гель Виферон;
- ношение медицинских масок в местах массового скопления людей;
- избегать путешествий в экзотические страны;
- предоставить вам доступ к медицинской помощи;
- не злоупотребляйте антибиотиками;
- пить чистую воду;
- овощи, фрукты и зелень тщательно вымыть, мясо разогреть.
Врага нужно знать в лицо
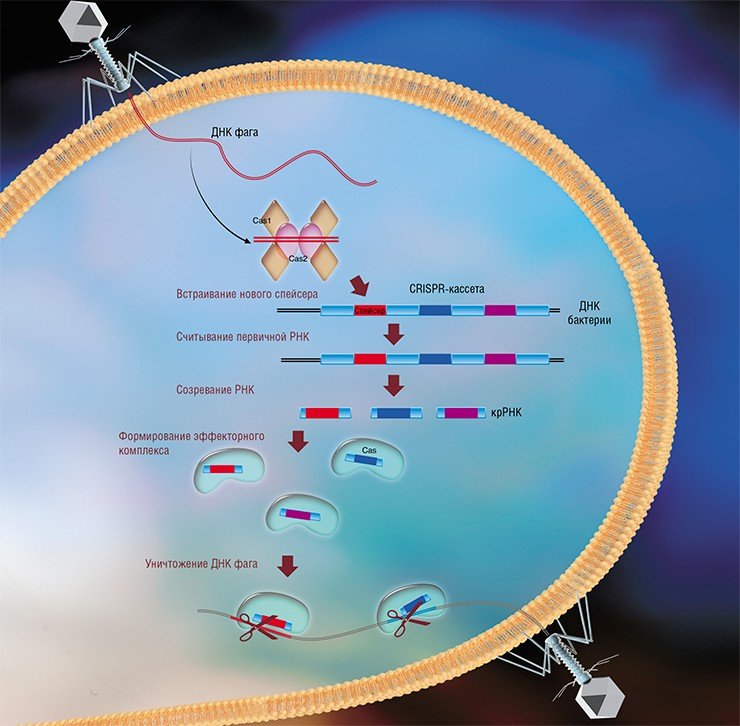
Системы CRISPR-Cas — уникальный пример адаптивного иммунитета у бактерий. Когда ДНК фага проникает в клетку, специальные белки Cas вставляют фрагменты вирусной ДНК длиной 25-40 нуклеотидов в определенную область бактериального генома (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. Spacer — пробел), область, где происходит встраивание, — кассета CRISPR (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс получения спейсеров является адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить другой Cas-контролируемый процесс, называемый интерференцией. Суть его в том, что при транскрипции кассеты CRISPR образуется длинная молекула РНК, которая отрезается от белков Cas на короткие фрагменты — защитные crispRNA (crRNA), каждый из которых содержит спейсер. Белки Cas вместе с молекулой crRNA образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие спейсер-идентичных последовательностей (протоспейсер). Обнаруженные протоспазиаторы расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas встречаются у большинства прокариот — бактерий и архей. Хотя общий принцип работы всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно различаться в деталях. Наибольшие различия проявляются в структуре и функционировании эффекторного комплекса, поэтому системы CRISPR-Cas делятся на несколько типов. К настоящему времени описано шесть типов таких несвязанных систем (Макарова и др., 2015; Шмаков и др., 2015).
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований — бактерия Escherichia coli. Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за различные функции: расщепление длинной некодирующей РНК CRISPR, связывание коротких crРНК, поиск и затем расщепление целевой ДНК.
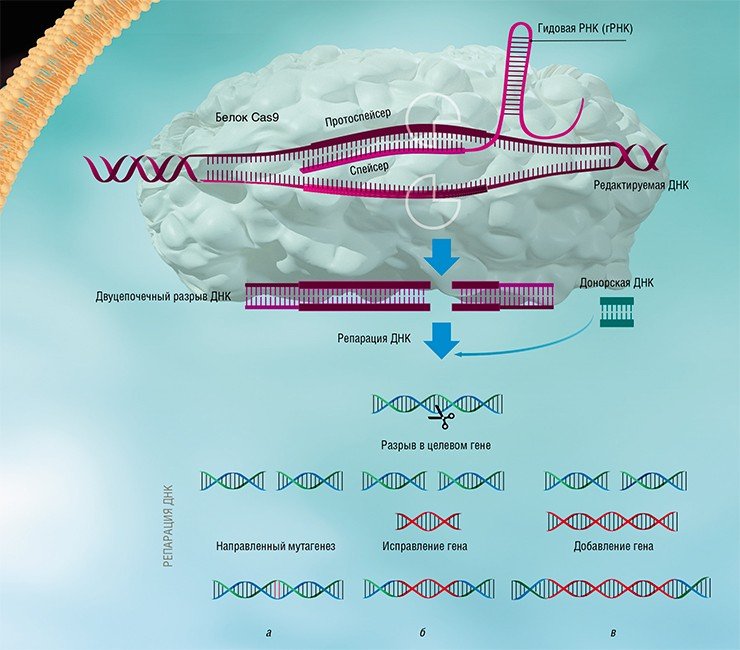
В системах типа II эффекторный комплекс образован одним крупным белком Cas9, который в одиночку справляется со всеми задачами. Именно простота и относительная компактность таких систем послужили основой для развития технологии модификации ДНК. Согласно этому методу, бактериальный белок Cas9 и crRNA, который называется проводником (gRNA), доставляется к эукариотическим клеткам (например, человека). Вместо спейсера вирусного происхождения такая гРНК содержит последовательность-мишень, соответствующую интересной для исследователя части генома, например, там, где есть мутация, вызывающая какое-то заболевание. Получить гРНК «на любой вкус» несложно.
Эффекторный комплекс Cas9-gRNA вводит двухцепочечный разрыв в последовательность ДНК, которая точно соответствует направляющей РНК. Если вместе с Cas9 и гРНК мы введем в клетку последовательность ДНК, не содержащую мутации, то локус гэпа будет восстановлен по «правильной» модели копирования! Таким образом, используя разные гРНК, можно исправить нежелательные мутации или внести целевые изменения в гены-мишени. Высокая точность запрограммированного распознавания целей комплексом Cas9-gRNA и простота метода привели к лавинообразному росту работ по редактированию генома клеток животных и растений (Jiang & Marraffini, 2015).
Гонка вооружений
В ходе эволюции бактерии и бактериофаги развили ряд приспособлений, которые должны дать каждому из участников «гонки вооружений» преимущество в борьбе с противником или возможность уклоняться от его атаки.
Бактериофаги, как факторы окружающей среды, вызывают направленные изменения в геноме бактерий, которые передаются по наследству и дают бактериям явное преимущество, спасая их от повторных инфекций. Таким образом, системы CRISPR-Cas можно рассматривать как пример ламарковской эволюции, в которой происходит наследование приобретенных признаков (Koonin et al., 2009)
Как и в случае с системами CRISPR-Cas, если фаг приобретает мутацию в протоспейсере, эффективность его распознавания эффекторным комплексом снижается, и фаг может инфицировать клетку. Но бактерии не проигнорируют такую попытку избежать CRISPR-Cas: в ответ они начнут приобретать новые дополнительные спейсеры из ДНК уже «знакомого», хотя и мутировавшего, фага со значительно повышенной эффективностью. Это явление, называемое триггерной адаптацией, многократно увеличивает эффективность защитного действия систем CRISPR-Cas (Даценко и др., 2012).
Некоторые бактериофаги реагируют на присутствие систем CRISPR-Cas в бактериальной клетке, продуцируя специальные белки анти-CRISPR, которые могут связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одна уловка — это замена участков вирусного генома, на которые нацелена система CRISPR-Cas, на участки генома родственных вирусов, которые различаются по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
Результаты работы нашей лаборатории показывают, что инфицированные клетки действительно умирают даже с защитой CRISPR-Cas, но в то же время ограничивают количество вирусных потомков. Следовательно, CRISPR-Cas более правильно относится к абортивным инфекционным системам, а не к «настоящим» иммунным системам.
В связи с постоянным совершенствованием алгоритмов исследования биоинформатики, а также включением в анализ все большего числа прокариотических геномов открытие новых типов систем CRISPR-Cas — дело ближайшего будущего. Более того, подробные механизмы работы многих недавно открытых систем еще предстоит уточнить. Например, в статье, опубликованной в 2016 году в журнале Science и посвященной анализу системы CRISPR-Cas типа VI, описан белок C2c2, который образует эффекторный комплекс с crRNA, направленный на деградацию не ДНК, а РНК (Abudayyeh et al., 2016)… В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемой ими РНК.
Изучение стратегий борьбы с бактериями с помощью бактериофагов, несмотря на очевидную фундаментальность и абстрагирование от задач практической медицины, принесло человечеству неоценимую пользу. Примерами являются методы молекулярного клонирования и модификации генома, то есть целенаправленное введение или удаление мутаций и изменений уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии, через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология редактирования генома, которая может бороться с заболеваниями, которые ранее считались неизлечимыми. Доступность и простота этой технологии позволяет считать ее основой медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, основанной на целевых и безопасных генетических модификациях.
Нет сомнений в том, что дальнейшие исследования взаимодействия бактерий и их вирусов могут открыть для нас возможности, о которых мы сейчас даже не подозреваем.
Наука и устойчивость
В настоящее время наиболее известными средствами борьбы с бактериями являются антибиотики, рождением которых мировое сообщество обязано Александру Флемингу, который в 1928 году в ходе исследований обнаружил, что обычная плесень Penicillium, растущая на черством хлебе, производит вещество, убивающее бактерии Семейство стафилококков.
так появился знаменитый «пенициллин».
Сегодня в мире существует несколько тысяч натуральных и даже синтетических антибиотиков, объединенных в 16 классов. Например, пенициллин — это бета-лактамный препарат.
Но из всего созданного ранее набора антибиотиков в настоящее время используется не более пяти процентов. Это напрямую связано с тем, что со временем у бактерий выработалась устойчивость к большинству этих препаратов.
Все это побудило ВОЗ после крупномасштабных исследований, проводимых с 2014 года, рассмотреть проблему устойчивости к противомикробным препаратам во всем мире и рекомендовать мировому научному сообществу начать поиск путей ее решения.
У ученых есть много идей, как бороться с проблемой: изучить механизмы возникновения устойчивости к противомикробным препаратам и системный мониторинг ее распространения, усовершенствовать меры по ограничению распространения и циркуляции патогенов с устойчивостью к противомикробным препаратам).
Среди них есть такой метод борьбы — научиться выращивать устойчивые виды бактерий и изучить химические соединения, с помощью которых устойчивость будет преодолена.
Эту проблему, в частности, решают ученые из Северо-Восточного университета в Бостоне (США). Им удалось найти ряд соединений, к одному из которых в лабораторных условиях ни одна из изученных бактерий не смогла выработать устойчивость.
И если говорить, например, о создании антибиотиков принципиально нового типа, то необходимо понимать, что, по мнению специалистов, на их разработку, прохождение всех этапов исследований и внедрение, по мнению специалистов, уходит в среднем 10 лет их в массовое производство.
В связи с этим ученые также ищут пути решения глобальной проблемы, основанные на противомикробных альтернативах антибиотикам.
Если говорить о нашей стране, то в 2017 году для этих целей была утверждена «Стратегия предотвращения распространения устойчивости к противомикробным препаратам в Российской Федерации на период до 2030 года».
Он предусматривает меры по ограничению распространения устойчивости микроорганизмов к противомикробным препаратам, химическим и биологическим агентам.
В частности, в стратегию интегрирован план действий по разработке и внедрению альтернативных методов, технологий, средств профилактики и лечения заболеваний, включая создание биологических препаратов на основе бактериофагов.
Борьба с вирусами и бактериями
полностью защититься от вирусов и бактерий невозможно. На человека постоянно нападает огромное количество микроорганизмов, и главный барьер на его пути — иммунитет. Поэтому важно укреплять и поддерживать иммунную систему в «боевом» состоянии, особенно в холодное время года и в периоды сезонных болезней.
Иммуномодулятор IRS®19 станет помощником на пути к здоровой и сильной иммунной системе. Содержит смесь лизатов бактерий, которые представляют собой специально изолированные части паразитарных бактерий. Лизаты активируют иммунную систему и направляют ее на борьбу с бактериями и вирусами. Препарат имеет высокий уровень безопасности и может назначаться для профилактики инфекций у взрослых и детей старше 3 месяцев. Он многократно тестировался и показал отличные результаты в борьбе с инфекциями, в том числе ОРВИ6.
